Že 24. avgusta 2021 sta Cara Therapeutics in njen poslovni partner Vifor Pharma objavila, da je FDA odobrila njihov prvi agonist kappa opioidnih receptorjev difelikefalin (KORSUVA™) za zdravljenje bolnikov s kronično ledvično boleznijo (KLB) (pozitiven zmeren/hud pruritus s hemodializnim zdravljenjem), njegov začetek prodaje pa je predviden v prvem četrtletju 2022. Cara in Vifor sta podpisala ekskluzivno licenčno pogodbo za komercializacijo zdravila KORSUVA™ v Združenih državah Amerike in se dogovorila za prodajo zdravila KORSUVA™ podjetju Fresenius Medical. Med njima imata Cara in Vifor vsak 60 % oziroma 40 % delež dobička v prihodkih od prodaje, razen Fresenius Medical; vsak ima 50 % delež dobička v prihodkih od prodaje podjetja Fresenius Medical.
S kronično ledvično boleznijo povezan pruritus (CKD-aP) je generaliziran pruritus, ki se pojavlja z veliko pogostostjo in intenzivnostjo pri bolnikih s kronično ledvično boleznijo, ki se zdravijo z dializo. Pruritus se pojavi pri približno 60 %–70 % bolnikov na dializi, od katerih ima 30 %–40 % zmeren/hud pruritus, ki resno vpliva na kakovost življenja (npr. slaba kakovost spanca) in je povezan z depresijo. Za srbenje, povezano s kronično ledvično boleznijo, doslej ni bilo učinkovitega zdravljenja, odobritev zdravila Difelikefalin pa pomaga odpraviti veliko vrzel v medicinskih potrebah. Ta odobritev temelji na dveh ključnih kliničnih preskušanjih faze III, ki so vložena v NDA: pozitivnih podatkih iz preskušanj KALM-1 in KALM-2 v ZDA in po svetu ter podpornih podatkih iz 32 dodatnih kliničnih študij, ki dokazujejo, da bolniki zdravilo KORSUVA™ dobro prenašajo.
Pred kratkim so prišle dobre novice iz klinične študije difelikefalina na Japonskem: 10. 1. 2022 je Cara objavila, da sta njena partnerja Maruishi Pharma in Kissey Pharma potrdila, da se injekcija difelikefalina na Japonskem uporablja za zdravljenje srbenja pri bolnikih na hemodializi. Klinična preskušanja faze III Primarni cilj je bil dosežen. 178 bolnikov je 6 tednov prejemalo difelikefalin ali placebo in sodelovalo v 52-tedenski odprti podaljšani študiji. Primarni cilj (sprememba ocene numerične lestvice ocenjevanja srbenja) in sekundarni cilj (sprememba ocene srbenja na Shiratorijevi lestvici resnosti) sta se v skupini, ki je prejemala difelikefalin, v primerjavi s skupino, ki je prejemala placebo, znatno izboljšala od izhodišča in bolniki so bolnike dobro prenašali.
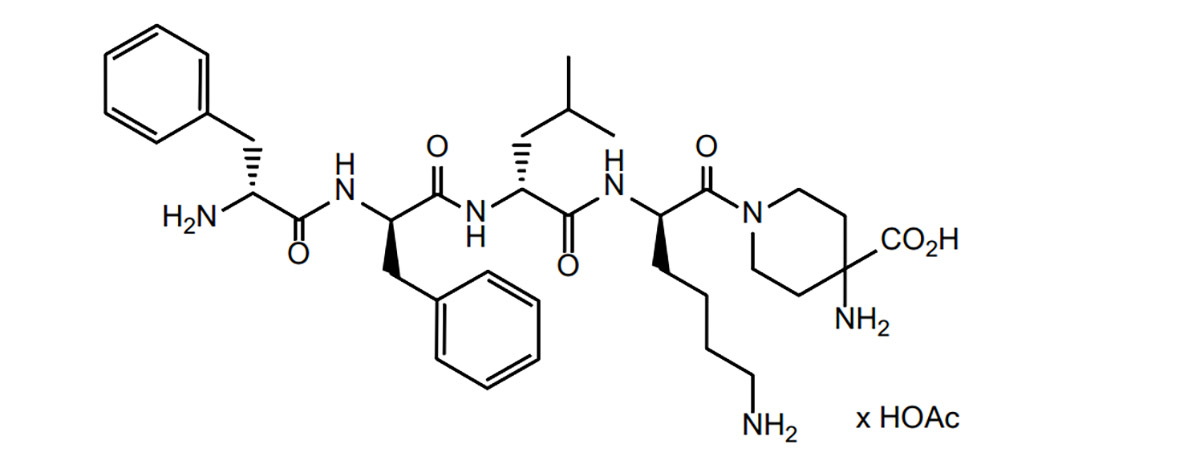
Difelikefalin je razred opioidnih peptidov. Na podlagi tega je Inštitut za raziskave peptidov preučil literaturo o opioidnih peptidih in povzel težave in strategije opioidnih peptidov pri razvoju zdravil, pa tudi trenutno stanje na področju razvoja zdravil.
Čas objave: 17. februar 2022